Istituto Zooprofilattico Sperimentale dell'Umbria e delle Marche. Perugia
Si ringrazia il Ministero della Salute che ha finanziato il Progetto IZSUM 07/2014 RC "Studio e controllo degli allergeni negli alimenti: valutazione e messa a punto di un metodo di conferma biomolecolare", Responsabile Scientifico Dott. Naceur Haouet.
Boyce JA, Assa'ad A, Burks AW, Jones SM, Sampson HA, Wood RA, Plaut M, Cooper SF, Fenton MJ, Arshad SH, Bahna SL, Beck LA, Byrd-Bredbenner C, Camargo CA Jr, Eichenfield L, Furuta GT, Hanifin JM, Jones C, Kraft M, Levy BD, Lieberman P, Luccioli S, McCall KM, Schneider LC, Simon RA, Simons FE, Teach SJ, Yawn BP, Schwaninger JM; NIAID-Sponsored Expert Panel (2010) Guidelines for the Diagnosis and Management of Food Allergy in the United States: Summary of the NIAID-Sponsored Expert Panel Report. J Allergy Clin Immunol. 126(6):1105-18. doi: 10.1016/j.jaci.2010.10.008.
Ludvigsson JF1, Leffler DA, Bai JC, Biagi F, Fasano A, Green PH, Hadjivassiliou M, Kaukinen K, Kelly CP, Leonard JN, Lundin KE, Murray JA, Sanders DS, Walker MM, Zingone F, Ciacci C. (2013) The Oslo definitions for coeliac disease and related terms. Gut. 62(1):43-52. doi: 10.1136/gutjnl-2011-301346. Epub 2012 Feb 16.
Taylor S.L. and Hefle S.L. (2005) Food allergies and intollerances. In: Modern Nutrition in Health and Disease, 10th ed., ed. M.E. Shils, M. Shike, A. C. Ross, B. Caballero, and R.J. Cousins, Lippincott, Williams and Wilkins, Philadelphia PA, pp. 1512-1530.
Manea I., Ailenei E., Deleanu D. (2016) Overview of food allergy diagnosis. Clujul Med. 89, 5-10. Doi: 10.15386/cjmed-513.
Ministero della Salute. Allergie alimentari e sicurezza del consumatore. Documento di indirizzo e stato dell'arte.
FNOMCeO. Allergie e intolleranze alimentari. Documento condiviso.
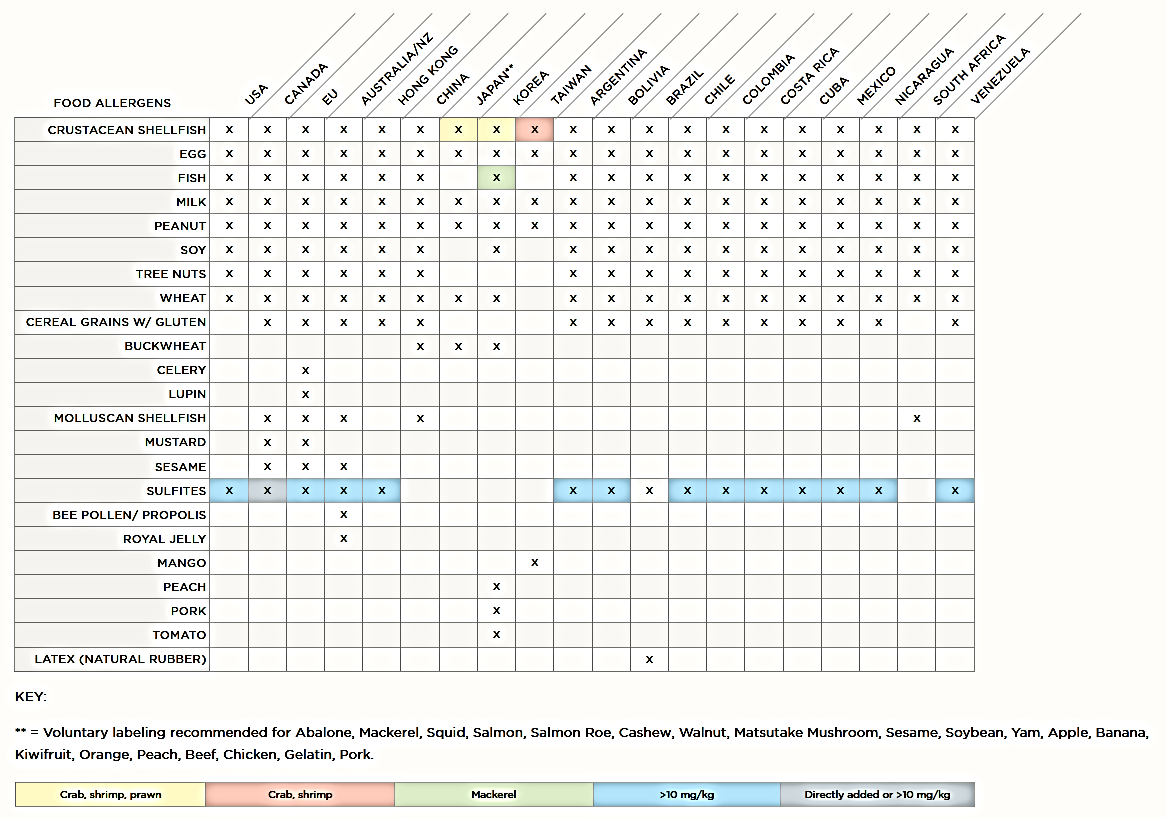
Gendel S.M. (2012) Comparison of international food allergen labeling regulations. Regulatory Toxicology and Pharmacology 63: 279-285.
DunnGalvin A., Chan C-H., Crevel R., Grimshaw K., Poms R., Schnadt S., Taylor S.L., Turner P., Allen K.J., Austin M., Baka A., Baumert J.L., Baumgartner S., Beyer K., Bucchini L., Fernandez-Rivas M., Grinter K., Houben G.F., Hourihane J., Kenna F., Kruizinga A.G., Lack G., Madsen C.B., Clare Mills E.N., Papadopoulos N.G., Alldrick A., Regent L., Sherlock R., Wal J-M, Roberts G. (2015) Precautionary allergen labelling: perspectives from key stakeholder groups. Allergy 70: 1039-1051.
Allen K.J., Remington B.C., Baumert J.L., Crevel R.W.R., Houben G.F., Brooke-Taylor S., Kruizinga A.G., Taylor S.L. (2014) Allergen reference doses for precautionary labeling (VITAL 2.0): Clinical implications. J.Allergy Clin. Immunol. 133, 156-164. Doi:10.1016/j.jaci.2013.06.042.
Taylor S.L., Baumert J.L., Kruizinga A.G., Remington B.C., Crevel R.W.R., Brooke-Taylor S., Allen K.J., Houben G. (2014) Establishment of Reference Doses for residues of allergenic foods: Report of the VITAL Expert Panel. Food Chem. Toxicol. 63, 9-17. Doi:10.1016/j.fct.2013.10.032.
Regolamento (UE) N. 1169/2011 DEL PARLAMENTO EUROPEO E DEL CONSIGLIO del 25 ottobre 2011 relativo alla fornitura di informazioni sugli alimenti ai consumatori, che modifica i regolamenti (CE) n. 1924/2006 e (CE) n. 1925/2006 del Parlamento europeo e del Consiglio e abroga la direttiva 87/250/CEE della Commissione, la direttiva 90/496/CEE del Consiglio, la direttiva 1999/10/CE della Commissione, la direttiva 2000/13/CE del Parlamento europeo e del Consiglio, le direttive 2002/67/CE e 2008/5/CE della Commissione e il regolamento (CE) n. 608/2004 della Commissione.
Regolamento (CE) N.178/2002 DEL PARLAMENTO EUROPEO E DEL CONSIGLIO del 28 gennaio 2002 che stabilisce i principi e i requisiti generali della legislazione alimentare, istituisce l'Autoritŕ europea per la sicurezza alimentare e fissa procedure nel campo della sicurezza alimentare.
Regolamento di esecuzione (UE) N. 828/2014 DELLA COMMISSIONE del 30 luglio 2014 relativo alle prescrizioni riguardanti l'informazione dei consumatori sull'assenza di glutine o sulla sua presenza in misura ridotta negli alimenti.
UNI CEN/TS 15634-2: 2012 Prodotti alimentari. Ricerca di allergeni alimentari mediante metodi di biologia molecolare. Parte 2: Sedano (Apium graveolens) - Determinazione qualitativa della sequenza di DNA specifica negli insaccati cotti mediante PCR in tempo reale.
EUR 24790EN 2011. Verification of analytical methods for GMO testing when implementing interlaboratory validated methods (ISBN 978-92-79-19925-7).
MPR 2015. Definition of Minimum Performance Requirements for Analytical Methods of GMO Testing. 20 October 2015.
Torricelli M., Pierboni E., Tovo G. R., Rondini C. (2016) In-house validation of a DNA extraction protocol from honey and bee pollen and analysis in Fast real-time PCR of commercial honey samples using a knowledge-based approach. Food Analytical Methods DOI: 10.1007/s12161-016-0539-x (Pubblicato on-line il 18 maggio 2016).
ISO 21571:2005/Amd.1:2013 "Foodstuffs - Methods of analysis for the detection of genetically modified organisms and derived products - Nucleic acid extraction".
Germini A., Scaravelli ·E., Lesignoli ·F., Sforza ·S., Corradini ·R., Marchelli R. (2005) Polymerase chain reaction coupled with peptide nucleic acid high-performance liquid chromatography for the sensitive detection of traces of potentially allergenic hazelnut in foodstuffs. Eur Food Res Technol 220:619-624 DOI 10.1007/s00217-004-1105-0.
Hird H., Lloyd J., Goodier R., Brown J., Reece P. (2003) Detection of peanut using real-time polymerase chain reaction Eur Food Res Technol 217:265-268 DOI 10.1007/s00217-003-0726-z.
Platteau C., De Loose M., De Meulenaer B., Taverniers I. (2011) Detection of Allergneic Ingredients Using Real-Time PCR: A Case Study on Hazelnut (Corylus avellana) and Soy (Glycine max). J. l of Agric. Food Chem., 59: 10803-10814.
Pierboni E., Curcio L., Tovo G.R., Torricelli M., Rondini C. (2016) Evaluation of Systems for Nopaline Synthase Terminator in Fast and Standard Real-Time PCR to Screen Genetically Modified Organisms. Food Analytical Methods, Volume 9, Issue 4, pp 1009-1019, doi: 10.1007/s12161-015-0283-7 (Pubblicato online: 14 agosto 2015).
Sitografia
EAACI, European Academy of Allergy & Clinical Immunology -
http://www.eaaci.org
FARE, Food Allergy Research & Education -
https://www.foodallergy.org/facts-and-stats
FARRP, Food Allergy Research and Resource Program -
http://farrp.unl.edu/reg-sit-food-allergens
MONIQA, International Association for Monitoring and Quality Assurance in the Total Food Supply Chain -
http://www.moniqa.org/
VITAL, Allergen Bureau | -
http://allergenbureau.net/vital/